2025新教材人教版高中化学(必修第一册)电子课本(最新高清pdf版-可下载打印)
开心田螺
2025-06-24 17:08:48
0次
人教版高中化学(必修第一册)电子课本可以方便大家随时随地预习或复习课本知识,为此,我们找到了人教版高中化学(必修第一册)新教材电子书教材的全部内容,以高清图片的形式呈现给大家,希望能够提高大家的学习效率。
如需全套电子课本PDF版,请关注公众号“桃李百科”回复:“电子课本”
人教版高中化学(必修第一册)新教材电子课本在线阅读(此为截图版,获取是高清版)












以下是 2025 新教材人教版高中化学必修第一册的期末知识点总结:
第一章 物质及其变化
- 物质的分类
- 元素与物质的关系:元素在自然界有游离态和化合态两种存在形式1。由同种元素组成的纯净物是单质,由多种元素组成的纯净物是化合物1。
- 同素异形体:同种元素形成的不同单质,如金刚石和石墨、氧气和臭氧等4。
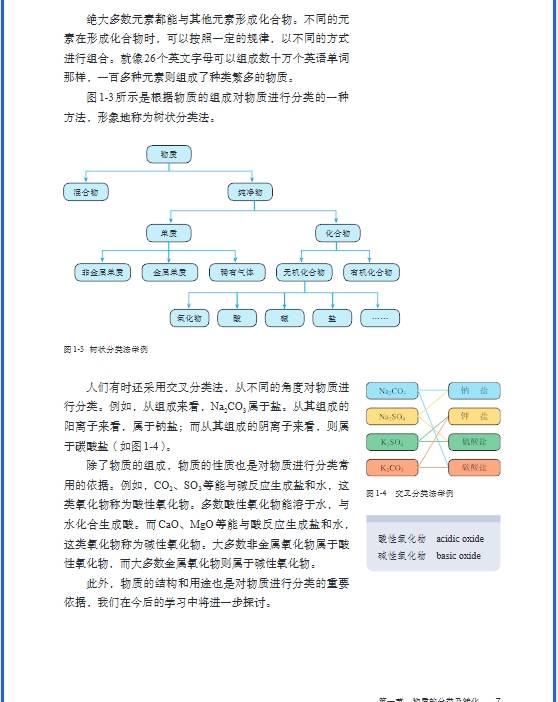
- 物质分类方法:树状分类法可将物质按组成等进行分类,交叉分类法能从不同角度对物质进行分类2。
- 分散系:一种(或多种)物质分散到另一种(或多种)物质中得到的体系。根据分散质粒子直径大小分为溶液、胶体和浊液,胶体粒子直径在 1 - 100nm 之间4。
- 物质的转化
- 酸、碱、盐的化学通性:酸能与酸碱指示剂、活泼金属、碱性氧化物、碱、盐反应;碱能与酸碱指示剂、酸性氧化物、酸、盐反应;盐能与酸、碱、盐反应2。
- 氧化物的化学通性:酸性氧化物能与水、碱、碱性氧化物反应;碱性氧化物能与水、酸、酸性氧化物反应2。
第二章 海水中的重要元素 —— 钠和氯
- 钠及其化合物
- 钠:具有强还原性,能与氧气、水等反应。与氧气常温下反应生成氧化钠,加热时生成过氧化钠;与水反应生成氢氧化钠和氢气。
- 钠的化合物:过氧化钠可与水、二氧化碳反应生成氧气,常用于呼吸面具和潜水艇中作为氧气的来源;碳酸钠和碳酸氢钠性质有差异,如在溶解性、热稳定性、与酸反应的剧烈程度等方面不同。
- 氯及其化合物
- 氯气:是一种黄绿色有刺激性气味的气体,具有强氧化性,能与金属、非金属、水、碱等反应。
- 氯的化合物:次氯酸具有强氧化性、漂白性和不稳定性,其酸性比碳酸弱;漂白粉的主要成分是氯化钙和次氯酸钙,有效成分是次氯酸钙,在空气中易与二氧化碳和水反应而变质。
第三章 物质的量
- 物质的量及其单位:物质的量是国际单位制中七个基本物理量之一,用于衡量一定数目粒子的集合体,单位是摩尔。
- 阿伏加德罗常数:1mol 任何粒子的粒子数叫做阿伏加德罗常数,近似值为\(6.02\times10^{23}mol^{-1}\)。
- 摩尔质量:单位物质的量的物质所具有的质量,单位是 g/mol。数值上等于该物质的相对原子质量或相对分子质量。
- 气体摩尔体积:在标准状况下,1mol 任何气体所占的体积都约为 22.4L,这个体积叫做气体摩尔体积。
- 物质的量浓度:以单位体积溶液里所含溶质 B 的物质的量来表示溶液组成的物理量,单位是 mol/L。
第四章 物质结构 元素周期律
- 原子结构:原子由原子核和核外电子构成,原子核由质子和中子构成。质子数决定元素的种类,质子数和中子数决定原子的质量数。
- 元素周期表:元素周期表有 7 个周期,16 个族。周期表中元素的位置与原子结构密切相关,同周期元素从左到右原子半径逐渐减小,金属性逐渐减弱,非金属性逐渐增强;同主族元素从上到下原子半径逐渐增大,金属性逐渐增强,非金属性逐渐减弱。
- 元素周期律:元素的性质随着原子序数的递增而呈周期性变化,主要体现在原子半径、化合价、金属性和非金属性等方面。
- 化学键:相邻原子间强烈的相互作用。包括离子键和共价键,离子键是阴、阳离子之间的静电作用,共价键是原子间通过共用电子对形成的相互作用。
相关内容
热门资讯
2026春沪教五四制版六年级数...
2026 春沪教五四制版六年级数学下册以 “数与代数拓展 + 几何直观培养” 为核心,涵盖分数运算深...
2026天津出国留学机构排名前...
随着2026年海外院校申请通道逐步开启,天津学子的留学规划进入关键阶段。在海量留学机构中,筛选出服务...
新年15岁少女“谷圈乱象”冲上...
这个世界越来越看不懂了。 最近刷到一条热搜,看得人满脸问号。 一个15岁的少女,竟然当着众人的面,死...
珲春成人高考招生专业
标题探索珲春成人高考招生专业,开启人生新篇章 在我国东北地区,有一个美丽的边境城市珲春。这里风光旖旎...
银发课堂还可以学点什么
近日,天津河北区消防救援支队联合区老年大学开设的消防安全培训课,以“趣味互动+实用教学”的形式吸引了...
2026年国考笔试成绩发布
来源:滚动播报 (来源:北京商报) 北京商报讯(记者 吴其芸)1月14日,据北京日报消息,2026年...
权威发布留学求职机构服务推荐:...
留学生求职服务作为连接海外学生与全球就业市场的专业桥梁,其核心价值在于整合企业招聘资源、导师辅导体系...
探索建筑的奇妙世界:联盟路小学...
为充分挖掘家长资源、拓展学生视野,推动家校共育、实现教育同频,联盟路小学“家长‘职’慧课堂”持续开展...
我市2025年冬季普通高中学业...
1月10日至11日,我市2025年冬季普通高中学业水平合格性考试在市第一中学标准化考点开考。本次考试...
中产家庭留学抉择:掏空家底换一...
最近后台收到不少家长的私信,核心问题都绕不开:“孩子该不该出国?这钱花得值不值?”作为一个在留学行业...
